Minha senha
Por favor digite seu email cadastrado em nosso sistema que enviaremos uma nova senha de acesso.
Atualizado em 22/06/2020
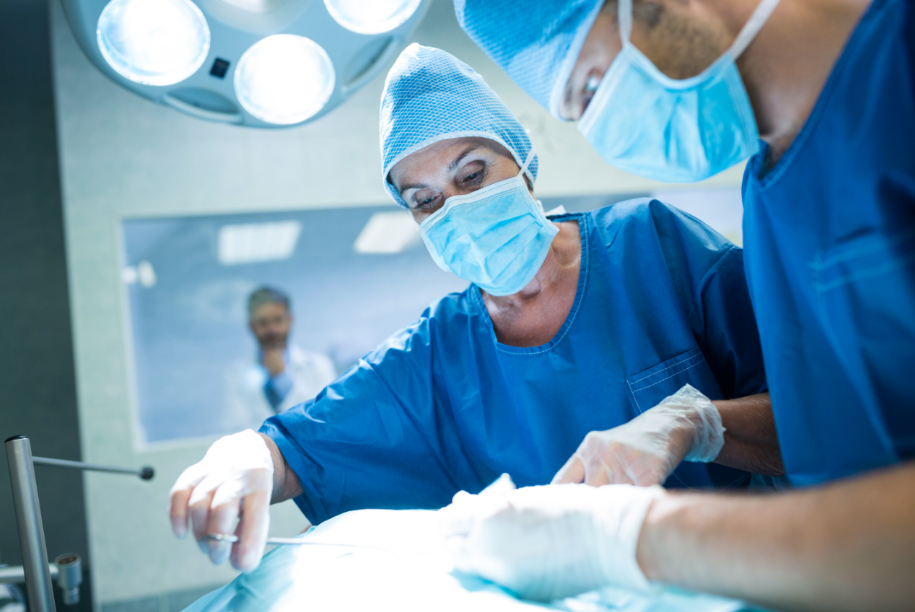

INTRODUÇÃO
O tratamento moderno do câncer de mama é baseado em uma abordagem multimodal, integrando cirurgia, radioterapia e terapia sistêmica, em combinações e sequências diferentes, dependendo da necessidade de cada paciente, com objetivo de de-escalonar os tratamentos, preservando a segurança oncológica.
A terapia sistêmica neoadjuvante (NST) é utilizada em cerca de 17-40% dos pacientes, com resposta patológica completa (pCR) adquirida em cerca de 20% deles, dependendo do subtipo tumoral. Nós já sabemos que pCR está associada a melhor prognóstico e que para pacientes não respondedores, o uso de terapia sistêmica pós neoadjuvância (TDM1 e capecitabina) melhora sobrevida.
Devemos pensar também em estratégias de tratamento locorregional mais personalizadas. Nas últimas quatro décadas, estudos mostraram que a cirurgia conservadora da mama é segura, com sobrevida semelhante a mastectomia, mesma após NST.
Seguindo esse raciocínio, parece lógico que o próximo passo será omitir a cirurgia no tratamento de câncer de mama de pacientes com resposta completa após NST e quatro principais questões guiam nosso raciocínio. Primeiro, quais são as medidas diagnósticas importantes para validar um teste para identificar pCR? Segundo, quais ferramentas diagnósticas podem detectar pCR com acurácia e menor morbidade possível? Terceiro, quais as consequências oncológicas de não identificar doença residual mínima e devemos aceitar a estratégia de watch-and-wait para pacientes com resposta completa pós NST? Quarto, como devemos desenhar e realizar estudos para ter evidência suficiente para mudar a prática clínica?
PRIMEIRO: MEDIDAS DOS RESULTADO DIAGNÓSTICO
O diagnóstico preciso de pCR é importante, pois sabemos que ela está relacionada diretamente com desfechos oncológicos.
Sensibilidade
Para predizer pCR, nós propomos a taxa de falso negativo (FN) como desfecho primário de um teste diagnóstico. Idealmente, a FN deveria ser zero, no entanto, esse objetivo é irreal na prática. Extrapolando os dados que já temos dos trabalhos de linfonodo sentinela pós NST, nós deduzimos uma sensibilidade mínima de 90% (FN máximo de 10%).
Especificidade
A especificidade também é relevante, considerando que é importante que o maior número de paciente se beneficiem do teste: a ferramenta diagnóstica deve identificar precisamente o maior número possível de pacientes com pCR para ser clinicamente válida.
SEGUNDO: FERRAMENTAS DIAGNÓSTICAS PARA CONFIRMAR DOENÇA RESIDUAL
A biópsia minimamente invasiva guiada por imagem tem mostrado resultados promissores na identificação de doença residual na mama e estudos têm investigado o método mais acurado para padronizar a abordagem futura. Alguns fatores parecem influenciar a acurácia: biologia tumoral; método de guiar o procedimento (estereotaxia ou ultrassom); espessura da agulha e número de fragmentos retirados.
Além disso, outro desafio é baseado no tipo de resposta tumoral a NST (“encolhimento” ou perda difusa celular) e na dificuldade de quantificar a real extensão da doença inicial e residual nos exames de imagem.
TERCEIRO: “PERDA” DE DOENÇA RESIDUAL
Eliminar a ressecção cirúrgica é oncologicamente seguro após a biópsia guiada por imagem demonstrar ausência de doença residual?
Existe conflitos de evidências sobre o impacto de não identificar doença residual após NST, mas o medo é certo: maior número de recorrências e piores desfechos de sobrevida. As consequências devem depender de alguns fatores: extensão da doença residual; doença residual invasiva ou in situ; e invasão angiolinfática. Nós acreditamos que a doença residual mínima pode ser suficientemente controlada por radioterapia e terapias sistêmicas pós neoadjuvância, como terapias anti-Her2 e hormonioterapia, quando indicadas.
Estudos recentes mostraram que em pacientes com doença residual, o uso de capecitabina ou TDM1, para pacientes triplo negativo e Her2 positivo, respectivamente, melhora sobrevida global e reduz o risco de recorrência. Nesses grupos, a “perda” de doença residual pode ter particular importância.
Racionalidade para eliminar a cirurgia
Em outros tipos de câncer, como câncer retal e esofágico, a estratégia de “watch-and-wait” já é utilizada após excelente resposta a NST. O efeito oncológico de uma possível doença residual mínima na mama é desconhecido, mas podemos comparar com pacientes com carcinoma oculto da mama, cujos dados reportam taxas de sobrevida semelhantes às outras pacientes com câncer de mama.
Como seguir as pacientes quando a cirurgia não é realizada? Como definir e tratar uma recorrência local?
Qualquer recorrência local deve ser considerada relevante em abordagens não cirúrgicas após NST. Nós sugerimos seguimento de rotina com exames de imagem de acordo com o padrão do serviço, além de ressonância magnética das mamas anual por pelo menos 5 anos (idealmente 10 anos). O acompanhamento com exames de imagem em intervalos mais curtos também pode ser considerado.
Além disso, os achados dos exames nesse novo cenário irão necessitar de monitoramento constante para encontrar um equilíbrio entre segurança e recomendação para exames adicionais (imagem ou biópsia) potencialmente desnecessários.
É interessante também avaliar a economia de recursos, considerando a abordagem não cirúrgica.
QUARTO: QUESTÕES RELACIONADAS A FUTUROS ESTUDOS CLÍNICOS
Existem alguns desafios práticos e metodológicos que devem ser considerados no desenho dos estudos. O primeiro é a dificuldade de atingir o número mínimo de pacientes necessários na amostra. O estudo deve ser controlado e randomizado, comparando as duas estratégias após NST: terapia padrão com cirurgia e radioterapia ou apenas radioterapia. Todos os outros tratamentos adjuvantes devem ser realizados de acordo com os guidelines. O desfecho primário deve ser recorrência locorregional; desfechos secundários devem incluir: aspectos econômicos e preferência da paciente.
O primeiro estudo, já iniciado e em andamento no MD Anderson, não é randomizado e tem uma amostra pequena e bem selecionado.
Randomizar as pacientes nesse contexto é um desafio, já que são duas abordagens muito diferentes. Permitir que o paciente escolha seu grupo de tratamento é uma estratégia mais centrada no paciente e coerente com os cuidados de saúde atuais, baseados em valores. Nesses casos, todas as variáveis com potencial influência no resultado final devem ser cuidadosamente documentadas. Além disso, possíveis trocas de abordagem durante o seguimento devem ser analisadas separadamente.
Considerando os resultados de trabalhos em andamento, que tentam identificar o método diagnóstico com maior acurácia e as mulheres com menor risco de recorrência e segurança oncológica, nós devemos discutir qual é o grupo de pacientes em que a omissão da cirurgia deve ser investigada em estudos futuros.
CONCLUSÃO
Nosso objetivo é descalonar a cirurgia em um subgrupo específico de pacientes, aumentando a qualidade de vida, sem causar danos. No entanto, não há atualmente nenhuma evidência que resolva essa questão e é um desafio conduzir um estudo clínico de qualidade nesse cenário.

Residência médica em Mastologia no Hospital Sírio Libanês Fellowship de Oncoplastia na Clique Rhena, Strasbourg, França Médica assistente da residência médica de Mastologia do Hospital Sírio Libanês Mastologista do Hospital São Camilo Pompéia Membro titular da Sociedade Brasileira de Mastologia